Pfizer kondigt aan dat het toch goedkeuring zal aanvragen voor een Lyme-disease vaccin, ondanks dat de latefase trial zijn statistische doel miste. Volgens Pfizer kregen te weinig deelnemers de ziekte om definitieve conclusies te trekken, maar het vaccin verminderde het infectierisico met meer dan 70% vergeleken met placebo. Het bedrijf noemt deze effectiviteit “sterk genoeg” om regulerende instanties te benaderen.
Annaliesa Anderson, Chief Vaccines Officer bij Pfizer zei:
De effectiviteit van meer dan 70% in de VALOR-studie is zeer bemoedigend en geeft vertrouwen in het vermogen van het vaccin om te beschermen tegen deze slopende ziekte.
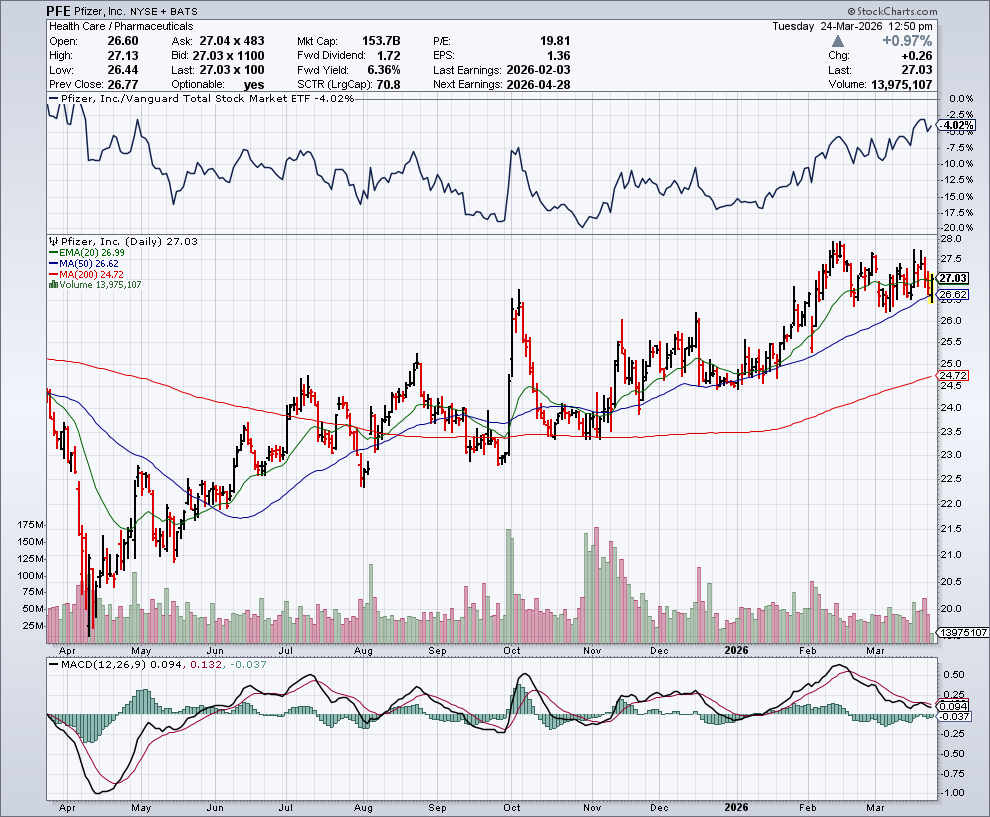
In de onderstaande grafiek zien we het koersverloop van Pfizer:
Potentie en uitdagingen van het vaccin
Het Lyme-vaccin van Pfizer, ontwikkeld samen met partner Valneva, kan volgens schattingen piekverkopen van meer dan $1 miljard per jaar halen.
Hoewel dit relatief klein is vergeleken met Pfizer’s totale jaaromzet van circa $60 miljard, zou het vaccin de eerste menselijke bescherming tegen Lyme in de VS kunnen bieden.
De trial kende uitdagingen: in 2023 werden ongeveer de helft van de deelnemers uit de Phase-3 studie gehaald vanwege kwaliteitsproblemen bij een externe trialsite. Uiteindelijk deden zo’n 9.400 mensen mee, van de oorspronkelijke 18.000.
Het vaccin richt zich op het outer surface protein A van de Lyme-bacterie. Gevaccineerde personen maken antilichamen aan die via teken de bacterieoverdracht naar mensen blokkeren.
Het schema omvat drie injecties in het eerste jaar en een booster in het tweede jaar. Pfizer en Valneva melden dat er in de trial geen veiligheidsproblemen zijn vastgesteld.
Met de voortzetting van de aanvraag testen ze ook het beleid van Amerikaanse regelgevers op strengere vaccincontroles, aangezien dit vaccin technisch gezien de trial niet volledig haalde.
Bron: CNBC
Foto: iStock